作者:张利桃,Charles River 维通利华 产品经理,lynn.zhang@criver.cn
维通利华hIL-15 NOG小鼠有效促进γδ T细胞在小鼠体内的续存和扩增,可加速γδ T细胞治疗的研究和开发。现货供应,点击咨询。
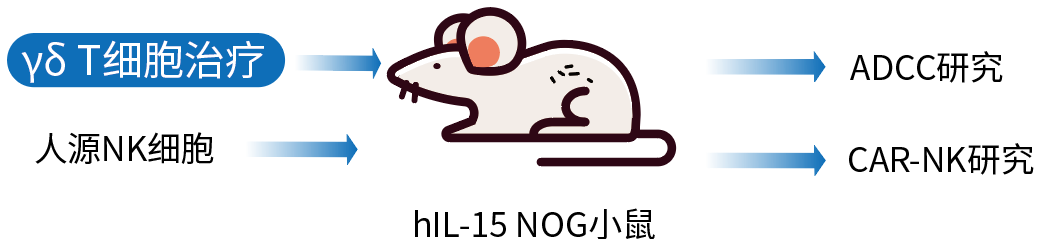
维通利华hIL-15 NOG小鼠:在超重度免疫缺陷小鼠NOG的基础上转入hIL-15,进一步缩小人鼠间免疫微环境的差异,助力新型免疫疗法的临床前验证。在之前的文章中,我们分享过hIL-15 NOG小鼠移植huNK后可以实现NK细胞在小鼠体内长时间的分化和增殖,为ADCC抗体药物及NK细胞疗法提供了合适的体内研究模型。这里,重点介绍hIL-15 NOG小鼠如何助力免疫治疗“新宠”—γδ T细胞的临床前评估。
IL-15属于四个α螺旋组成的14~15 kD的四聚体家族,是一种多效性细胞因子,不仅能在CD8 + T细胞、NKT细胞和NK细胞的发育、激活和存活中发挥重要作用,同时也能促进γδ T细胞的激活和增殖[1, 2]。维通利华现有的hIL-15 NOG小鼠(日本CIEM研发)稳定持续表达人源细胞因子IL-15,促进γδ T细胞在小鼠体内的存续和扩增,已有研究表明,与市场上同类模型相比,其能更好地助力γδ T细胞疗法的临床前研究。
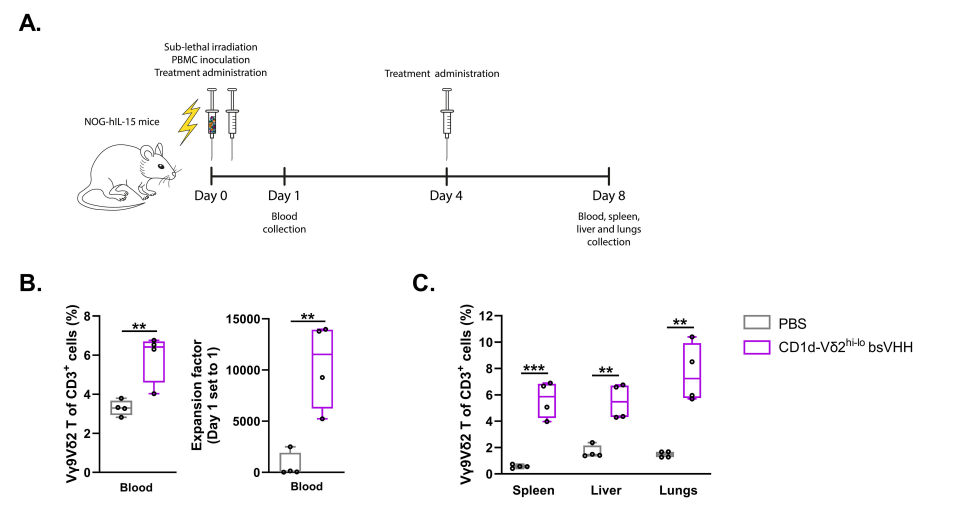
hIL-15NOG小鼠静脉注射人源外周血单个核细胞(huPBMC)后,注射CD1d-Vδ2hi-lo bsVHH可诱导小鼠外周血、脾脏、肝脏和肺脏组织中Vγ9Vδ2 T细胞的扩增[3]。
2023年强生的下属公司杨森生物技术公司(Janssen Biotech, Inc.)在世界知识产权组织(WIPO)申请获批了一项在免疫细胞治疗领域具有重要参考价值的专利:《用于提升改进免疫细胞扩增和使用的材料和方法》。在研究中其发现,与美国JAX的NSG或NSG-hIL-15小鼠相比,日本CIEM研发的hIL-15 NOG小鼠移植细胞后展示更强更持久的γδ T细胞的存续和扩增能力[4]。
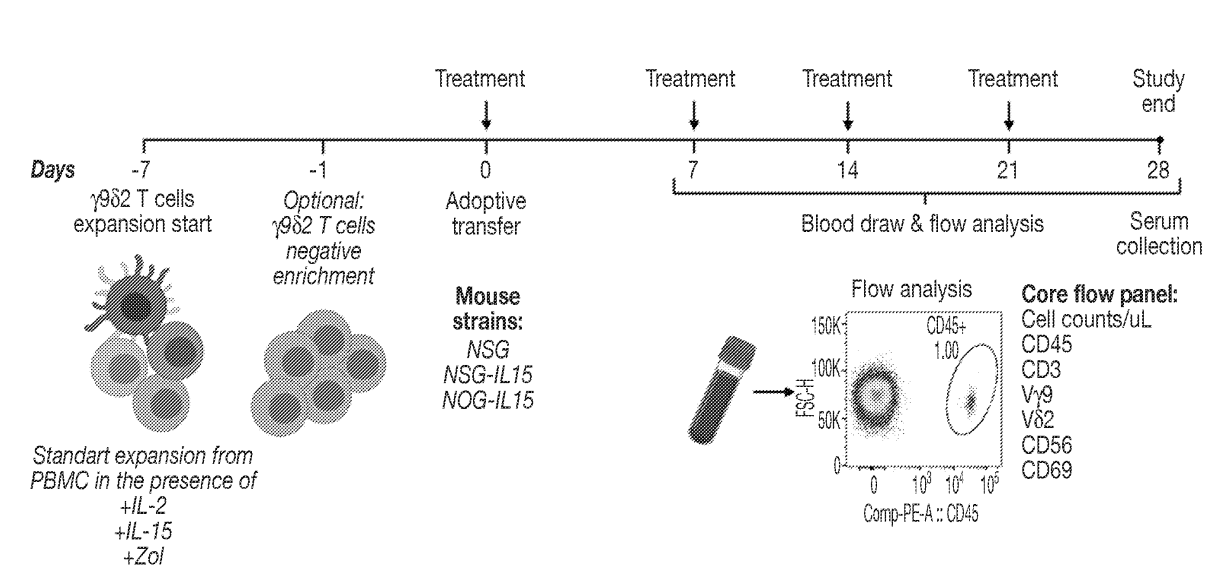
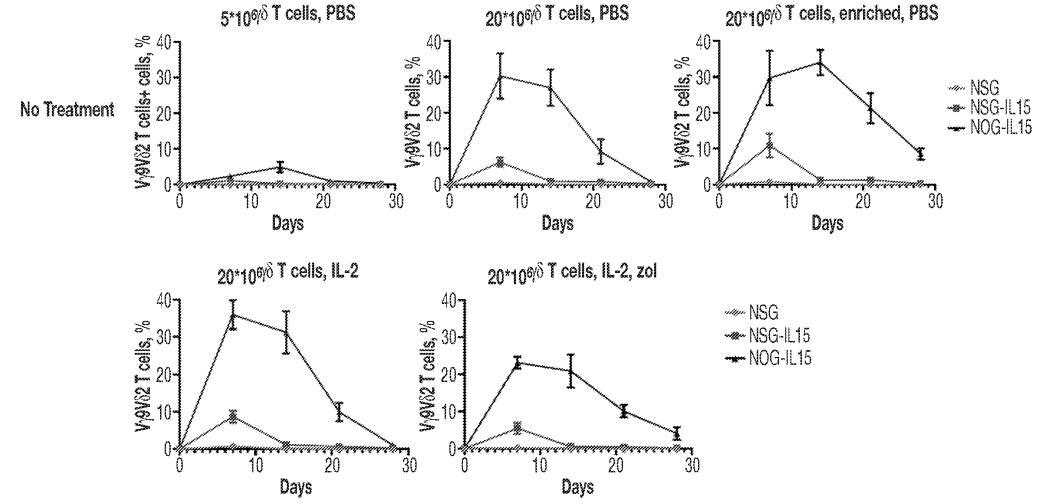
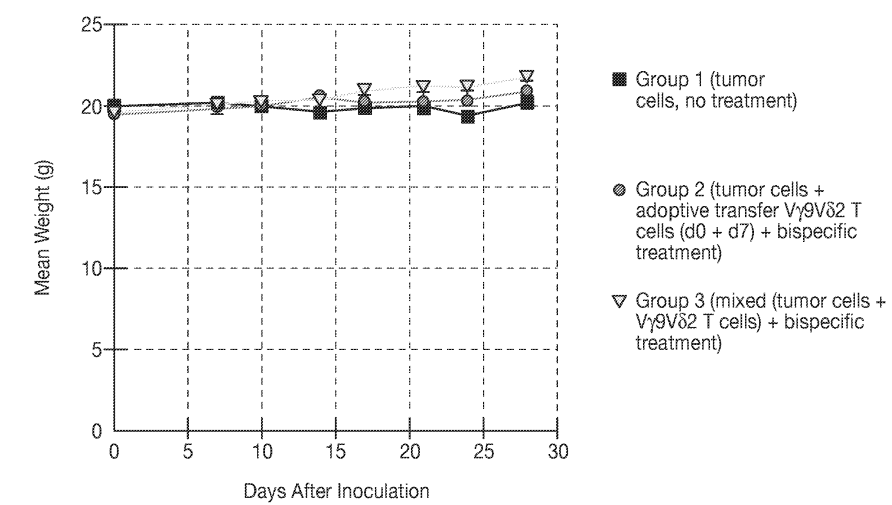
进一步的特异性双抗的药效显示,NOG-hIL15小鼠分别静脉移植纯化的Vγ9Vδ2+ T细胞和皮下移植肿瘤细胞株,或同时皮下注射Vγ9Vδ2+ T细胞和肿瘤细胞株,分别进行特异性双抗干预后,有显著的抑瘤效果,说明Vγ9Vδ2+ T细胞可以浸润到肿瘤内部发挥作用,且实验期间各组小鼠体重维持恒定,没有GvHD反应发生。
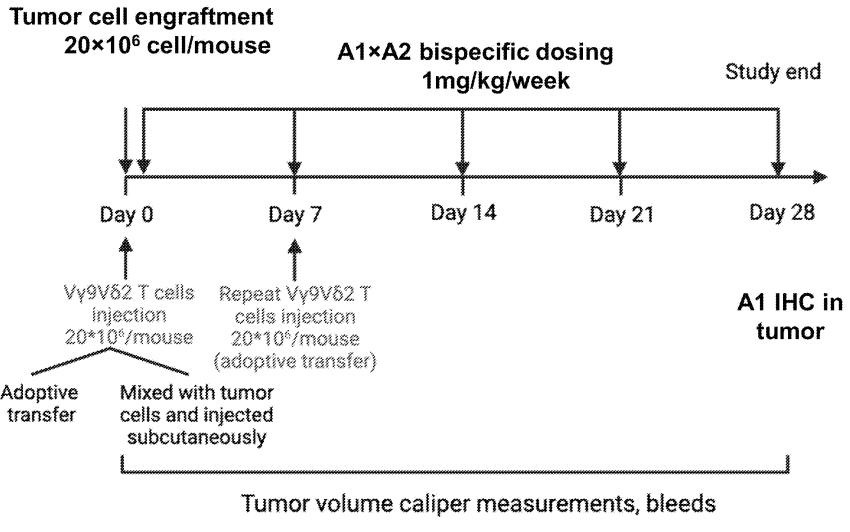
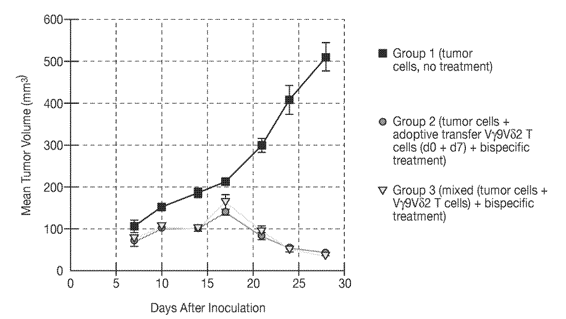
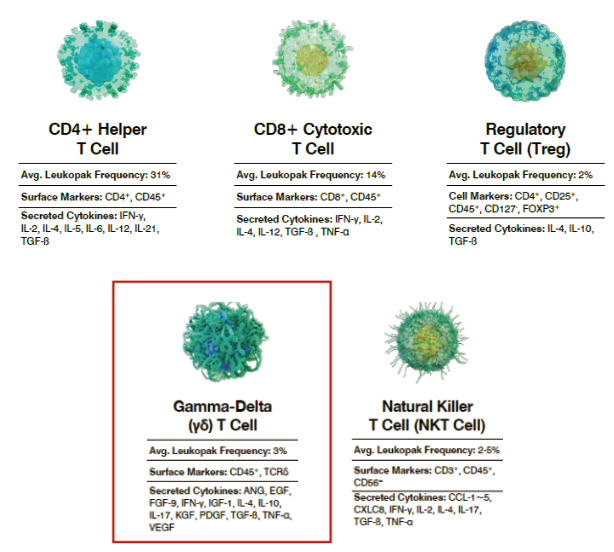
在人类外周血中,αβT细胞是T细胞的主体细胞,是当前CAR-T细胞的主要来源。γδ T细胞虽然含量很低,占总T细胞的1%至5%,但其优势非常明显:1)其通过TCR依赖的机制进行抗原识别而非MHC依赖性,因而具有广泛的肿瘤识别能力;2)通过释放炎性细胞因子如干扰素-γ和颗粒酶及穿孔蛋白等直接杀伤肿瘤细胞表现出强大的抗肿瘤活性;3)γδ T细胞能耐受低氧、低糖的肿瘤微环境;4)安全有效,因为γδ T细胞的非MHC限制性,所以几乎没有GvHD(移植物抗宿主病)反应发生。多项研究报道,其已在免疫治疗领域显示出巨大的潜力和应用前景[5]。
2024年10月,美国癌症中心发表在《Cell Reports Medicine》的研究对来自TCGA数据库中33种癌症类型的11000个肿瘤样本的γδ T细胞受体(γδ TCR)进行全面分析,揭示了γδ T与患者预后的相关性。尽管γδ T占比少,但γδ T细胞能够识别更广泛的肿瘤抗原,在治疗不同的实体瘤和血液瘤上都有独特的优势[6]。
2024年12月,Francis Crick研究所的Adrian Hayday等人《Science》上,发表了一篇题为“Cancer immunotherapy by γδ T cells”的综述文章,深入剖析了γδ T细胞在癌症治疗中的独特优势(非MHC限制性识别抗原、广泛的肿瘤识别能力、组织趋向性、多重作用机制)、利用γδ T细胞进行癌症治疗的多种临床试验进展和创新型疗法等应用前景[7]。
2024年4月28日,国内首个基于γδ-T细胞的创新免疫细胞药物:广东暨德康民自主研发的用于治疗原发性肝细胞癌的创新细胞药物γδ T细胞注射液获得了国家药品监督管理局药品审评中心的临床试验默示许可。
近年来,γδ T细胞已经成为肿瘤免疫细胞治疗领域的“新黑马”,维通利华提供的现货hIL-15 NOG小鼠,因其超重度免疫缺陷的特性和持续性表达适宜浓度的hIL-15,可有效促进γδ T细胞在小鼠体内的续存和扩增。这些特性使得hIL-15 NOG小鼠成为临床前研究中评估γδ T细胞肿瘤免疫疗法效果的重要工具,极大地促进了新疗法评估和肿瘤免疫治疗领域的发展。
产品咨询:Product@criver.cn
订购hIL15-NOG模型
订购电话:010-84744555
订购邮箱:Order@criver.cn
NK细胞研发加速计划:看hIL-15 NOG小鼠推动细胞疗法新进展
https://mp.weixin.qq.com/s/yqiW5_eef1fAxXDaZxQ-ww
寻找NK细胞相关体内研究模型?hIL-15 NOG小鼠给你答案!
https://mp.weixin.qq.com/s/NnR-nUMfWobDWUjuA9jm6g
1. Van Acker HH, Anguille S, Willemen Y, Van den Bergh JM, Berneman ZN, Lion E, et al. Interleukin-15 enhances the proliferation, stimulatory phenotype, and antitumor effector functions of human gamma delta T cells. J Hematol OncolJ Hematol Oncol(2016) 9(1):101. doi: 10.1186/s13045-016-0329-3
2. Wang X, Zhao XY. Transcription factors associated with IL-15 cytokine signaling during NK cell development. Front Immunol(2021) 12:610789. doi:10.3389/fimmu.2021.610789
3. King et al. Vδ2 T-cell engagers bivalent for Vδ2-TCR binding provide anti-tumor immunity and support robust Vγ9Vδ2 T-cell expansion. Front. Oncol., 2024 Oct 18, Volume 14. doi.org/10.3389/fonc.2024.1474007
4. GORDON, Renata, et al. MATERIALS AND METHODS FOR IMPROVED EXPANSION AND USES OF IMMUNE CELLS. WO/2023/086968.
5. Di Carlo, E.; Bocca, P.; Emionite, L.; Cilli, M.; Cipollone, G.; Morandi, F.; Raffaghello, L.; Pistoia, V.; Prigione, I. Mechanisms of the Antitumor Activity of Human Vgamma9Vdelta2 T Cells in Combination with Zoledronic Acid in a Preclinical Model of Neuroblastoma. Mol. Ther. 2013, 21, 1034–1043.[CrossRef][PubMed]
6. Yu et al., Pan-cancer gd TCR analysis uncovers clonotype diversity and prognostic potential. Cell Rep Med. 2024 Oct 4;5(10):101764. doi: 10.1016/j.xcrm.2024.101764
7. Hayday et al. Cancer immunotherapy by γδ T cells. Science. 2024 October 04; 386(6717): eabq7248. doi:10.1126/science.abq7248.