作者:Regina Kelder
Charles River的科学家们如何利用这些小型化体外系统的力量作为动物试验的潜在替代方案
七年前,癌症专家朱莉娅·舒勒(Julia Schueler)在勃林格殷格翰(Boehringer Ingelheim)度过了为期八周的休假,其中涉及大量移液。化学家和生物学家都知道这是一项繁琐的任务,但对于Charles River实验室训练有素的兽医和肿瘤学治疗领域负责人 Schueler 来说,这是值得的,因为她有机会近距离了解 BI 在维也纳的全球癌症中心如何使用称为类器官的 3D 细胞培养物。
Schueler位于德国弗莱堡的实验室专门研究患者来源的异种移植物或PDX模型 - 携带来自患者肿瘤的组织或细胞的小鼠,为持续生长创造环境 - 现在正在从这些小鼠化身中开发类器官。“我们的想法是拥有一种与PDX一样异质的体外工具,但仍然不含动物,”Schueler说。“我们目前正在推动的项目是建立一个肺癌类器官组合,其中包括七个冷肿瘤(那些不太可能引发强烈免疫反应的肿瘤)和七个热肿瘤,我们知道这些肿瘤在体内的表现。Schueler补充说,将肿瘤分为热和冷对个体患者的治疗方案有直接影响。“在临床前研究中同时代表两组,可以提高哪些患者群体可能从新药中受益最多的预测强度。
弗莱堡还计划增加乳腺癌类器官,其位于北卡罗来纳州三角研究区的姊妹站点正在研究开发结肠癌类器官。Schueler说,最终目标是能够为客户提供一种有效的方法来识别人类特异性药物靶点和疾病机制,甚至为个体患者找到最佳治疗方法。
癌症并不是查尔斯·里弗类器官研究的唯一焦点。莱顿研究中心的靶点发现计划跨越多个疾病领域,已经开发出可以评估胃肠道药物毒性的肠道类器官,他们最近启动了一项生成肝脏类器官以评估肝毒性的计划,肝毒性是大多数药物通过和代谢的器官。与此同时,Portishead工厂正在开发一个扁桃体类器官平台,用于测试疫苗和免疫调节剂。
Buti说,目前类器官最重要的作用之一是成为药物成功或失败的早期预测指标,这最终为客户节省了资金并减少了下游临床责任。“我们想及早发现'坏人',但我们也不想过滤掉实际上可能是一种真正好的药物。基本上,拥有这种更好地模仿患者生理机能的[类器官]系统,我们可以更好地控制我们所做的决定,“莱顿高级研究负责人Ludovico Buti博士说。
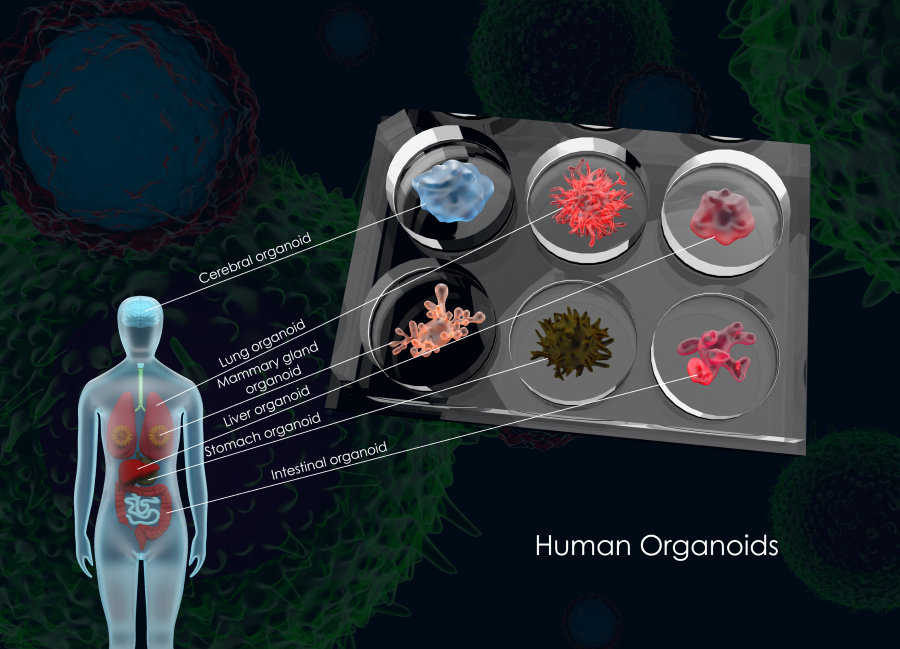
类器官是源自干细胞(人类,胎儿或成人)的 3D 细胞培养物,它们自组织并产生器官特异性细胞类型,旨在模仿人体器官的结构、功能和细胞复杂性,使它们在某些方面比与人类基因组成相似但不相同的动物更易于翻译。类器官的大小从小于头发的宽度到五毫米不等,并且由于它们来自干细胞,因此可以随着时间的推移在其培养物中扩增。这些体外小型化的器官非常适合研究复杂的器官,如大脑、肺、肾脏或胰腺,现在广泛用于学术实验室研究器官发育。
类器官有时会与器官芯片混淆,但平台实际上是完全不同的。虽然类器官的生长和自我组装与人体器官非常相似,但器官芯片是高度工程化的人造系统,其中生物成分(细胞)受到组织特异性微结构(工程部件)的影响。类器官缺乏器官芯片所具有的微流体环境和拉伸能力,但包含大部分生物成分。鉴于两者的进步,科学家们正在探索将类器官和器官芯片一起使用以获得更好结果的方法也就不足为奇了。
为了创造类器官,科学家们将多能细胞嵌入到蛋白质和其他分子的大型细胞外网络中,这些分子为细胞和组织提供结构。特定的生长因子和蛋白质维持干细胞的表型或功能。根据使用的初始干细胞群和添加的特定生长因子,基质中的细胞将开始组装成 3D 类器官结构,其行为类似于目标的特定组织。
类器官于1987年由加州大学伯克利分校和丹佛的实验室首次开发,此前取得了两项重要的科学成功:应用了一种对分解受损组织中的胶原蛋白和帮助健康组织生长很重要的酶,以及分离出一种称为基质胶的凝胶状蛋白质混合物,该混合物支持诱导多能干细胞(iPS)细胞的维持。随着时间的推移,类器官的准确性和可重复性都得到了提高,今天类器官是二维细胞模型的有效替代品。2009年,由Hans Clevers(现任罗氏制药、研究和早期开发负责人)领导的荷兰一个研究小组开发了一种针对人类肠道类器官的改良培养条件,可提高培养效率并保持其长期多分化能力。两年后,辛辛那提大学的科学家能够从iPSC开始,并概括为肠道类器官的完全分化。
2016年,研究人员从囊性纤维化患者的细胞样本中制作了类器官,并使用3D模型来预测哪些患者会对新药产生反应。在 COVID 大流行期间,肺类器官被用于研究细胞微生物学问题并筛选新疗法和疫苗。
随着类器官被公认为药物开发中的新替代方法之一,公司现在为在临床前药物评估中使用它们敞开了大门。事实上,许多大型制药公司,如阿斯利康、罗氏和葛兰素史克都投资了类器官研究。尽管类器官和其他非动物模型仍处于起步阶段,但越来越多的证据表明,它们可以帮助降低临床前研究的成本和时间,并提高临床成功的几率,目前每10种药物中就有9种因疗效低下或意外毒性而失败。

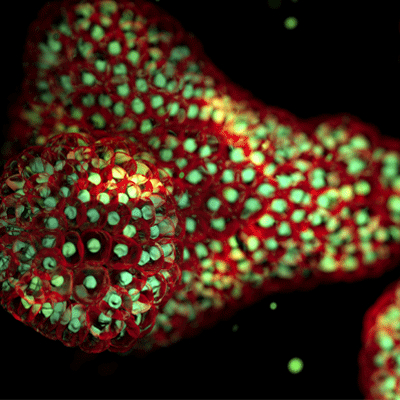
Intestinal organoid grows up in 7 days. 肠道类器官在 7 天内长大(Qun Wang)
Buti在莱顿的团队首先开始对类器官进行实验,作为OrganoVIR的一部分,OrganoVIR是一个由欧盟资助的联盟,旨在研究类器官中的人类病毒感染。“我们主要想了解这个3D模型的平移方面是什么,”Buti说。“我们知道,药物发现中的高流失率已不再可持续。我们想要了解的是,与细胞系相比,使用类器官的附加值是什么,然后将其与患者的情况进行比较。
他们通过与专门研究肠道病毒的生物学家学术小组合作来做到这一点,肠道病毒通常发生在胃肠道轨道上,但也可以攻击中枢神经系统和其他器官。Buti说,他们用肠道病毒A71菌株概括了类器官的感染,这是手足口病的常见原因。目前尚无批准的药物用于治疗这种感染,进入临床试验的少数实验化合物表现不佳。研究人员将这些失败的化合物与肠道类器官和2D细胞系进行了测试。去年发表在《细胞》杂志上的这个项目的研究结果很能说明问题。“在细胞系中,这三种化合物都效果很好,但是当我们使用类器官进行相同的练习时,三种化合物中的两种表明它们要么不够有效,要么毒性太大,或者两者兼而有之,”Buti说。“这仅说明,对于类器官,我们在药物发现过程的早期就引入了一个额外的过滤器。基本上,拥有这个模仿患者生理机能的[类器官]系统,可以让我们更好地控制我们所做的决定。
Buti说,与OrganoVIR的合作建立了使用类器官评估肠道中抗病毒药物毒性的概念验证。但他补充说,肠道类器官的价值远不止于此。“特别是当你想到肿瘤学领域时,化疗往往在肠道中具有毒性,”他说。“这些现在可以在类器官中进行测试,并帮助你在进一步开发药物之前对药物的毒性做出明智的决定。
Image of a 3D organoid扁桃体类器官的使用是另一个研究的热门领域,它正逐渐接近商业可行性。三年前,斯坦福大学领导的一项研究展示了如何使用人类扁桃体开发一种类器官,该类器官在体外概括了生发中心的几个关键特征 - 感染或疫苗接种时在淋巴结中形成的结构。研究小组展示了他们如何使用这种类器官系统来定义产生流感疫苗反应所需的基本细胞成分。韩国研究团队还使用人扁桃体上皮类器官作为 SARS-CoV-2 感染的离体模型。
Charles River的波蒂斯黑德研究中心专门从事涉及免疫学、免疫肿瘤学和病毒学的发现研究,正在多个方面对扁桃体类器官进行实验,Charles River生物治疗部门的研究负责人Dan Rocca博士说。他说,这些领域包括使用类器官来更好地预测人类对治疗性抗体、基因疗法或细胞疗法的反应,就像斯坦福大学团队使用扁桃体类器官来预测对流感疫苗的反应一样。Portishead正在研究的另一个关键领域是使用人类扁桃体类器官来产生治疗性抗体。
“你可以使用小鼠模型或噬菌体展示平台来发现抗体,”Rocca说。“但是对于小鼠,你必须使用非常复杂的遗传模型,比如人源化小鼠,如果你采用噬菌体方法,你必须拥有超级优化的系统,这些系统是可用的。真正补充这些方法的是,如果你在人体系统中发现了抗体。扁桃体类器官可能被用来做到这一点。
例如,Rocca说,如果你把一种作为治疗靶点的癌症蛋白放入扁桃体类器官中,理论上你应该能够产生针对它的抗体反应。“然后,你可以通过分离扁桃体类器官产生的一些B细胞来克隆这种抗体,并拥有一种与真人相同的人类抗体。它还将代表一个更具生理相关性的系统,用于测试旨在改变免疫系统的药物,特别是T细胞或B细胞反应。我们才刚刚开始真正探索它的潜在用途。
类器官在临床前药物开发中的速度将取决于用户和监管机构对将工具数据整合到IND包中的信心。类器官的进步还需要生物制药公司和合作伙伴的坚实财务承诺,以及技术的持续改进。使用多组学进行全面表征,以了解药物靶标表达和生理相关性,这可能是一项庞大而昂贵的任务。
但窗户肯定是敞开的。Schueler说,她的团队已经与对PDX肺类器官感兴趣的公司进行了接触。Buti说,Charles River现在能够提供其肠道类器官平台,用于早期药物评估,以及疾病建模和靶点验证。由于许多大型制药公司已经在类器官模型上投入了金钱和时间,Buti表示,客户将科学外包给具有专业知识的合同合作伙伴将很有价值。
此外,新的工具正在开发中,使类器官更易于使用。今年4月,旨在将现实生活中的患者药代动力学引入实验室的δypha联盟获得了欧洲创新委员会和中小企业执行机构的250万欧元赠款,用于与包括Charles River在内的国际最终用户一起验证Sync Biosystems技术。Sync系统旨在减少培养细胞中使用自动移液器引起的应力和湍流。这种风切变对于类器官和其他类型的 2D 和 3D 细胞系统的用户来说是一个重大挑战;同步系统将这种干扰降至最低,同时允许将类器官与微流体系统相结合,从而实现药效学测试。
虽然类器官的增长是显而易见的,但它们是否会完全取代动物还有待观察。 “我希望如此,但现在我看到这个模型更多地是为了测试不同的条件,否则你将无法在体外测试,然后基本上缩小到一两个将在动物模型中测试的选项,”Buti说。“从这个意义上说,从短期来看,我看到了减少动物在研究中使用的潜力,因为类器官将帮助研究人员在早期寻找看起来最有前途的[药物]。
罗卡对此表示同意,并表示确保炒作不会领先于科学也很重要。“我认为所有这些新技术的问题在于,尽管它们显示出前景,但它们仍在由科学界开发,特别是用于药物开发,因此在我们能够完全取消动物试验之前,需要投入相当大的精力进行验证和测试 - 尽管这是我们所有人都在努力的事情。
查看替代方法推进项目 (AMAP),详细了解 Charles River 用于引领行业进入药物发现和开发的下一个前沿的科技创新。