CAR-T 作为活的细胞类药物,进行临床前体内研究时会引起Xeno-GvHD反应,不能进行长时间的药效评估,且药效评估的准确性也受到影响。
本文将介绍一种新型品系:NOG-MHC I/II-2 KO (NOG-dKO) 小鼠,huPBMC移植或CAR-T 药物处理后无明显的xeno-GvHD,可准确评估PD-1等免疫检查点抑制剂、双特异性抗体、组合疗法以及CAR-T/TCR-T药物的抗肿瘤活性。
CAR-T作为一种特殊的细胞类药物,建立临床前肿瘤模型时,需要提前考量更多的因素,如体内研究中动物模型对CAR-T药物的排斥反应。所以,研究者们在评价人肿瘤特异性T细胞,如过继性肿瘤特异性T淋巴细胞,CAR-T或TCR-T细胞的抗肿瘤作用时,研究者经常使用重度免疫缺陷小鼠,如NOG、NSG和NOD/SCID小鼠等,原因在于NOG小鼠对CAR-T药物的排斥较低,这对细胞治疗药物的临床前药效研究有非凡的意义。我们在与客户合作的研究项目中也发现血液瘤CAR-T研究使用超重度免疫缺陷小鼠NOG优势更明显。
然而,研究者发现由于CAR-T等T细胞药物在NOG、NSG小鼠中会出现xeno-GvHD反应(移植物抗宿主病),使得小鼠状态差难以进行长时间的药效评估;另外,这也一定程度转移了部分真正用于抗肿瘤作用的T细胞药物。CAR-T的研究者们在的实验研究中也会遇到类似问题,有时一些治疗窗口期较长的研究难以为继,并且有时这种xeno-GvHD反应会与CAR-T药物的脱靶副反应混淆,无法区分。
NOG-dKO小鼠,敲除了在xeno-GvHD反应发挥重要作用的分子,Tomonori Yaguchi et al.已在研究中证实NOG-dKO小鼠可以更准确评估CAR-T药物的抗肿瘤活性。
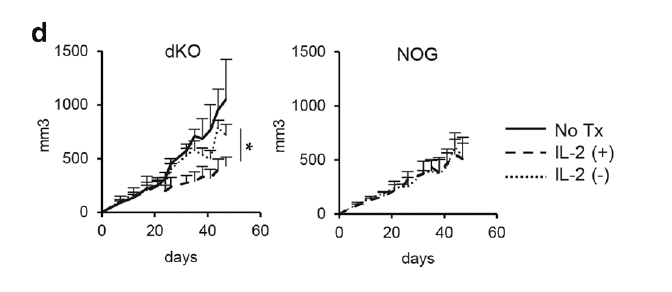
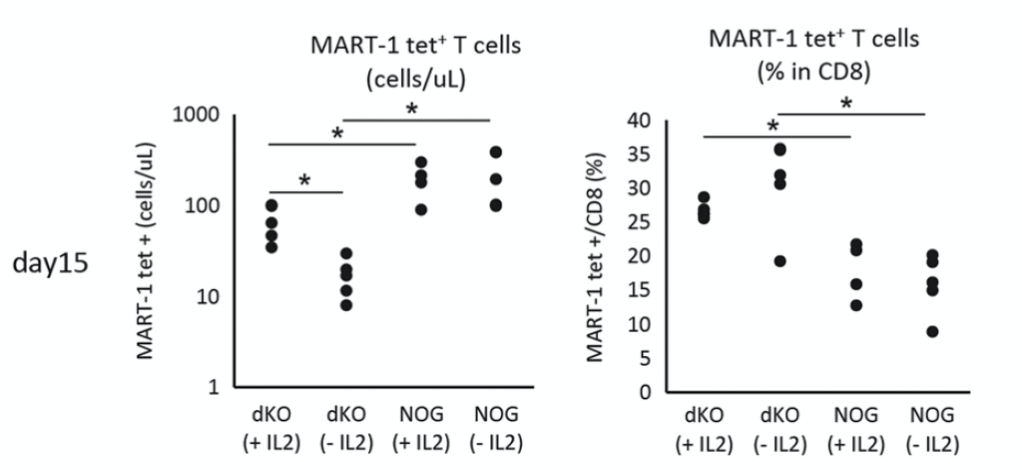
Tomonori Yaguchi利用NOG-dKO小鼠来评估MART-1-特异性T细胞对人类黑色素瘤(表达MART-1的526 mel细胞系)的杀伤作用,发现MART-1-特异性T细胞给药后,NOG-dKO小鼠表现出明显的抗肿瘤效应,且无体重丢失,进一步结合外源性IL-2细胞因子给药后,MART-1特异性T细胞的存活时间延长,抗肿瘤作用也进一步增强。利用NOG小鼠,虽然也表现出较多的T细胞浸润及较强的抗肿瘤效应,但给药后20-30天,动物体重开始急速下降,在给药后40天左右动物开始出现死亡;结合外源性IL-2细胞因子给药后也未出现明显的肿瘤抑制作用;浸润到肿瘤内部的CD8+特异性T细胞比例也要低于NOG-dKO小鼠,从侧面反映出,在NOG小鼠中出现的T细胞扩增及对肿瘤的抑制,一部分来源于Xeno-GVHD, 而非真正的T细胞药物活性。
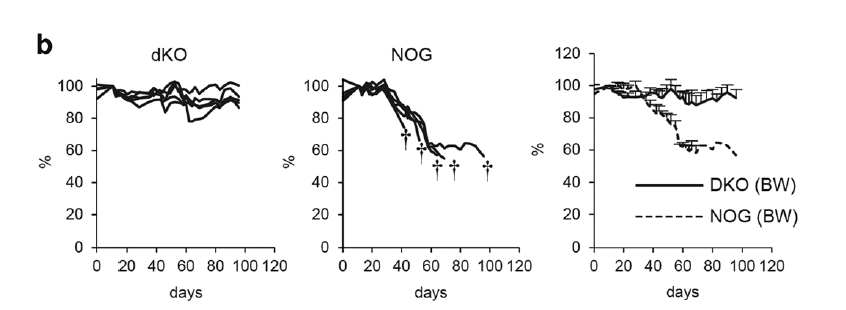
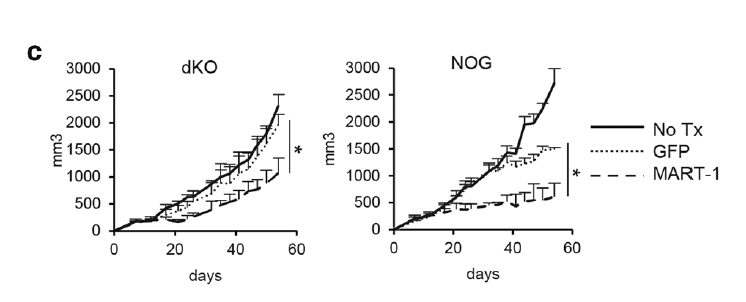
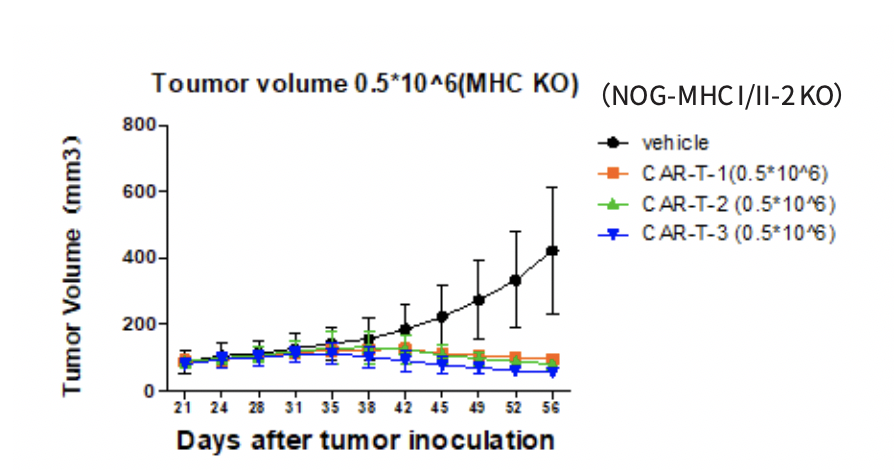
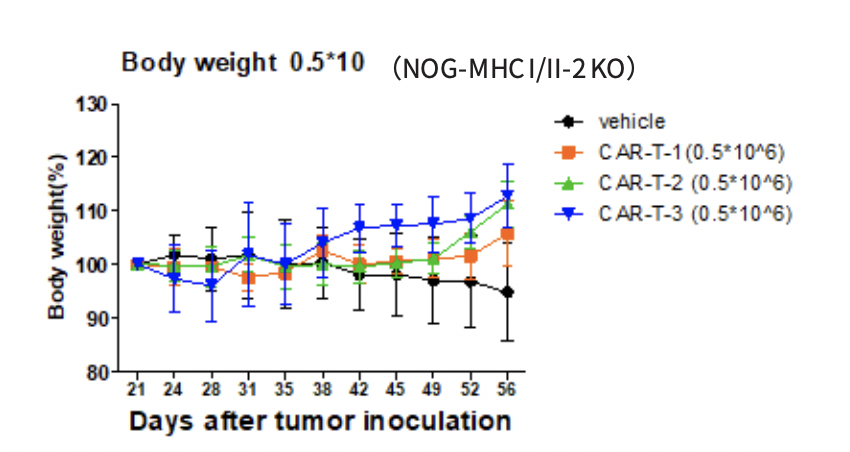
我们的合作单位使用NOG-dKO小鼠进行CAR-T药物人卵巢癌的研究,小鼠皮下接种1*10⁵的细胞系 SKOV3-PDL1(表达 PDL1 的人卵巢癌细胞系),肿瘤体积达到80-150mm3时给予CAR-T药物,发现CAR-T给药组肿瘤体积明显下降,且整个研究周期中(长达8周),小鼠体重未出现明显变化。
1) CAR-T/TCR-T药物处理后无Xeno-GvHD, 可助于CAR-T药物长时间的临床前药效评估;
2) 可避免Xeno-GvHD反应会与CAR-T药物的脱靶副反应混淆;
3) 避免由于Xeno-GvHD造成的CAR-T药物浪费,也能解释肿瘤的抑制不是由于Xeno-GvHD导致,可准确地评估CAR-T药物的临床前抗肿瘤活性。
维通利华NOG-dKO小鼠已经量产,现货充足!

[1]. Yaguchi et al.: MHC class I/II deficient NOG mice are useful for analysis of human T/B cell responses for human tumor immunology research. Journal for ImmunoTherapy of Cancer 2013 1(Suppl 1):P39.
[2]. Tadashi, Ashizawa, Akira, et al. Antitumor Effect of Programmed Death-1 (PD-1) Blockade in Humanized the NOG-MHC Double Knockout Mouse.[J]. Clinical cancer research : an official journal of the American Association for Cancer Research, 2017.
[3]. Iizuka A , Nonomura C , Ashizawa T , et al. A T-cell-engaging B7-H4/CD3 bispecific Fab-scFv antibody targets human breast cancer[J]. Clinical Cancer Research, 2019.
[4]. Akiyama Y , Nonomura C , Ashizawa T , et al. The anti-tumor activity of the STAT3 inhibitor STX-0119 occurs via promotion of tumor-infiltrating lymphocyte accumulation in temozolomide-resistant glioblastoma cell line[J]. Immunology letters, 2017, 190.
[5]. Yaguchi T , Kobayashi A , Inozume T , et al. Human PBMC-transferred murine MHC class I/II-deficient NOG mice enable long-term evaluation of human immune responses[J]. Cellular & Molecular Immunology, 2017.