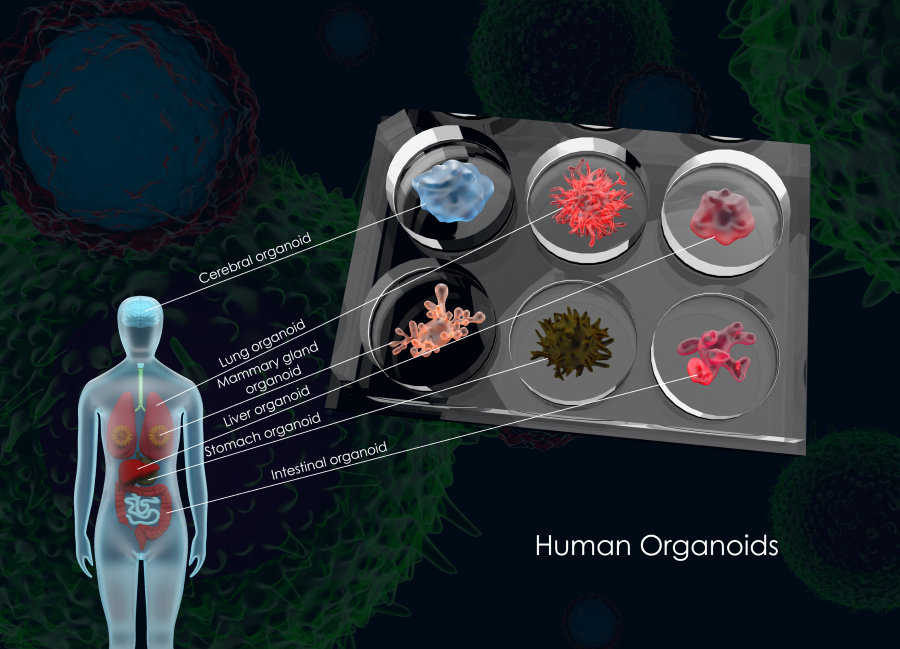
作者:宫世玲,Charles River 维通利华 高级产品经理, Shiling.Gong@criver.cn
重度免疫缺陷大鼠SRG(Sprague-Dawley background, Rag2-/-, Il2rg-/-), 在之前的讲述中已了解到该模型结合大鼠及重度免疫缺陷的特性,使其在肿瘤学研究中有独特的优势,弥补了重度免疫缺陷大鼠的空白。
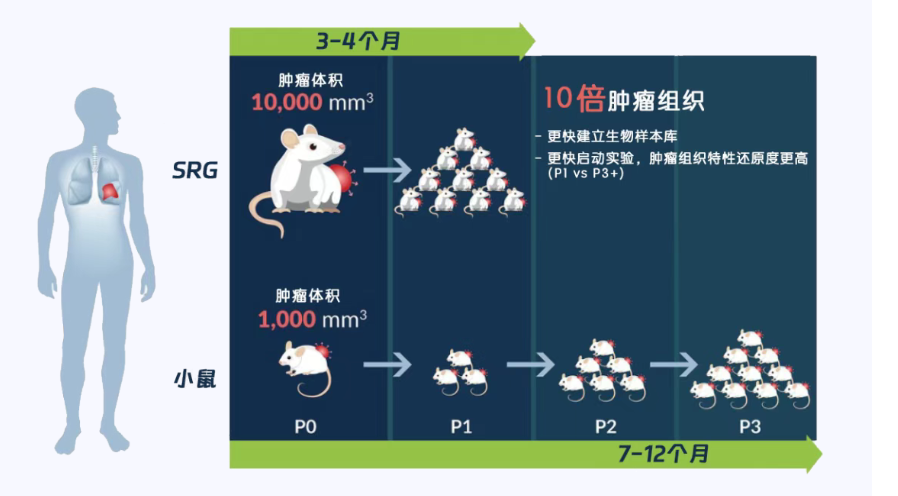
除此之外,我们来一起看看近一年内最新的重要文章,SRG大鼠给肿瘤学及再生医学研究带来的研发启示。
多项研究表明,与小鼠相比,SRG大鼠更能支持多种人类癌症类型的生长,并表现出更好的肿瘤微环境相互作用,且SRG大鼠生长的肿瘤中更发达的间质室和血管室更接近原始患者肿瘤的结构。乳腺癌研究中特别强调了大鼠在HR信号、乳腺结构、肿瘤病变的导管起源和激素依赖状态等方面与人类更相似。因此大鼠可以作为乳腺癌研究的最佳模型。
DOI: 10.1101/2025.03.27.645250
文章中作者对2种细胞来源细胞株(CDX)和7种患者来源的肿瘤组织(PDX)(包括前列腺癌、肺癌、卵巢癌和子宫癌)分别皮下植入SRG大鼠和N*G小鼠,并追踪肿瘤生长情况,发现SRG大鼠的植入效率和肿瘤生长速度均优于N*G小鼠。SRG大鼠的免疫受损并不比N*G小鼠更弱,表明其支持肿瘤生长存在其他机制。研发者进一步研究发现,在SRG大鼠中生长的肺癌PDX模型血管和基质形成增强,且形态学上与原患者肿瘤更一致。NCI-H660 CDX模型的免疫组化分析显示,肿瘤间质、脉管系统和巨噬细胞在两种宿主物种中存在差异。单细胞空间成像显示,与N*G小鼠相比,SRG大鼠生长的NCI-H660肿瘤中人类CXCL2和TCIM上调,二者均与癌症预后不良有关。
研究结果表明,与N*G小鼠相比,SRG大鼠更能支持多种人类癌症类型的生长,并表现出更好的肿瘤微环境相互作用。此外,SRG大鼠生长的肿瘤中更发达的间质室和血管室更接近原始患者肿瘤的结构,这强调了SRG大鼠作为人类癌症有价值模型的潜力。
DOI: 10.1007/s10911-024-09566-0
该文章中提到虽然激素受体阳性(HR+)乳腺癌(BC)小鼠模型已成为乳腺癌临床前体内模型的重要工具。然而,小鼠和人类之间乳腺系统和生物学的物种特异性差异突出了在乳腺癌研究中需要更准确和有代表性的模型。与小鼠相比,大鼠在HR信号、乳腺结构、肿瘤病变的导管起源和激素依赖状态等方面与人类更相似。因此大鼠可以作为乳腺癌研究的最佳模型。
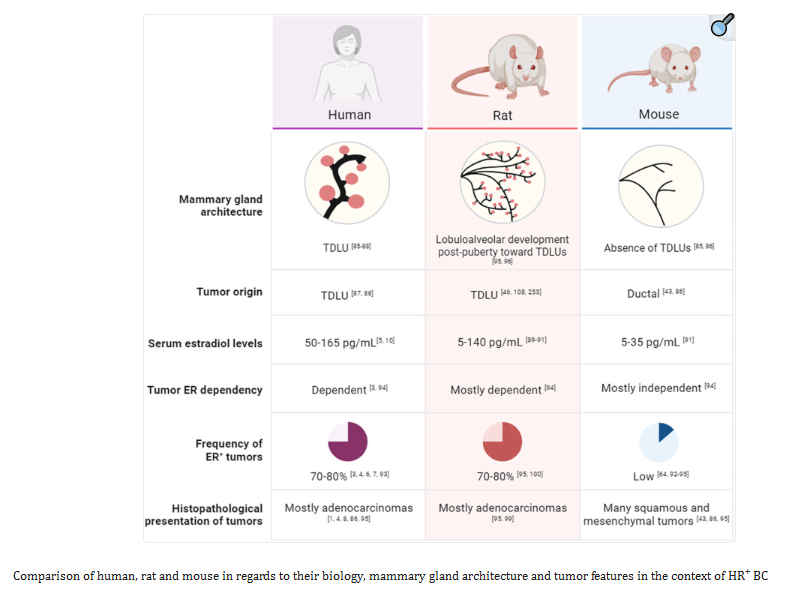
图注:人、大鼠和小鼠在HR+ BC背景下的生物学、乳腺结构和肿瘤特征的比较
这篇文章进一步综述了迄今为止六种不同类型的HR+ BC(激素受体阳性乳腺癌)大鼠模型。这些模型包括自发性、致癌物诱导、异种移植、激素诱导、辐射诱导和基因工程大鼠乳腺肿瘤模型。在异种移植模型中,SRG大鼠因其缺乏成熟的T细胞、B细胞和NK细胞,表现出严重的免疫缺陷,是一种近交系大鼠模型。SRG大鼠不仅对人类乳腺癌细胞系(如HCC1954)具有100%的移植成功率,还能够支持患者来源的异种移植物的建立和扩增。此外,SRG大鼠模型不仅适用于人类细胞系和患者来源的异种移植,还可用于小鼠到大鼠的细胞异种移植,这凸显了该模型的通用性及其在乳腺癌体内研究中的应用前景。
多项研究表明,SRG大鼠不仅可以提高PDX建模效率,同时在肿瘤原位移植/转移移植中优势突出:超重度免疫缺陷及与人更相似的生理结构,使得建模成功率高;同时体型大,可更方便及更容易建立原位及转移模型,且可进行广泛的纵向血液采样和肿瘤活检,进行后续研究。
Cancer Res (2024) 84 (6_Supplement): 1453.
https://doi.org/10.1158/1538-7445.AM2024-1453
本研究中使用SRG大鼠成功地建立PC3M-luc前列腺癌皮下及转移模型,且能够更好地模拟前列腺癌的临床转移,并很好地评估了紫杉醇和卡铂单药及联合用药的治疗效果。SRG大鼠在本研究中的优势是其体型大,可更好地建立原位及转移模型,且可进行广泛的纵向血液采样和肿瘤活检,用于药效学分析。
DOI: 10.1016/j.ejca.2024.114548
本研究利用SRG大鼠分别成功建立了人类胶质母细胞瘤细胞系U87MG-luc的大鼠大脑纹状体原位移植模型,脑转移性乳腺癌肿瘤的脑原位PDX模型和弥漫性内生型脑桥胶质瘤(DIPG)患者来源PDX模型。通过在体生物发光成像、MRI和组织学多方面数据显示肿瘤在SRG大鼠大脑中稳健生长。
这些数据证实了SRG大鼠是研究不同类型脑癌原位移植的优秀宿主。由于其较大的体型,与小鼠模型相比,支持更高的肿瘤负荷及移植效率,使得SRG大鼠在颅内原位肿瘤移植或者其他原位移植研究中具有很高的实用性。
SRG大鼠是在CD®(SD)大鼠背景上开发的免疫缺陷模型,可在同一背景品系下进行药效、药代动力学和毒理学研究,研究数据证明了SRG大鼠在癌症研究领域的潜力。
Cancer Res (2024) 84 (6_Supplement): 4183. https://doi.org/10.1158/1538-7445.AM2024-4183
高度免疫缺陷 SRG 大鼠在荷瘤动物中进行联合药效、药代动力学和毒理学研究的用途
该文章的研究数据表明,SRG大鼠是在CD®(SD)大鼠背景上开发的免疫缺陷模型。与CD大鼠相比,SRG大鼠除了在淋巴组织和白细胞数量上有所减少外,其余病理学特征基本相似。重要的是,SRG大鼠能够支持人类癌症组织的生长,并可进行多次样本采集,支持药效评估。这些研究数据证明了SRG大鼠在癌症研究领域的潜力:可在同一背景品系下进行药效、药代动力学和毒理学研究的潜力。
SRG大鼠由于其免疫缺陷特性及人更相似的生理结构,在组织缺损造模及更好的支持干细胞等细胞治疗药物的移植方面有极大的优势。
iScience. 2024 Jul 18;27(8):110537.
DOI: 10.1016/j.isci.2024.110537
本文的核心研究内容是是探索时间和细胞特异性激活骨形态发生蛋白(BMP)信号通路在限制软骨细胞肥大化中的作用,并开发一种新的方法来促进稳定透明软骨的形成。研究主要围绕人类骨髓基质干细胞/骨骼干细胞(hBMSCs/SSCs)和人类诱导多能干细胞(hiPSCs)展开,旨在为退行性软骨疾病提供更有效的细胞治疗策略。文章中SRG大鼠不仅作为体内移植模型验证了hiPSCs衍生软骨细胞的稳定性和有效性,还为未来软骨修复和再生医学的研究和临床应用提供了重要的参考。同时,也表明SRG大鼠可以应用于人类诱导多能干细胞(hiPSCs)的其他领域的再生医学研究。
JB JS Open Access. 2025 Jan 15;10(1):e24.00043.
DOI: 10.2106/JBJS.OA.24.00043
本文的研究背景是当前软骨修复疗法效果有限,而两栖动物(如蝾螈)的IZN组织能够再生大型关节损伤,哺乳动物在胎儿发育期间存在类似的组织,且在体外表现出显著的软骨生成能力。故研究中进一步使用SRG大鼠评估了胎儿软骨祖细胞(IZN和ANL细胞)在修复骨软骨缺损中的再生能力。
SRG作为一种免疫缺陷大鼠,不仅能够很好地在膝关节中创建骨软骨缺损,且由于其重度免疫缺陷,可以用于评估不同细胞类型的治疗修复效果,有助于优化细胞治疗策略,促进再生医学研究。
更多SRG相关文献汇总,在此不一一赘述,可登录维通利华官网查询:
https://www.vitalriver.com/rm-find-model/415-srg.html
总体而言,SRG大鼠由于其与人类更相似的生理学、更高的移植效率、更方便的移植或者手术操作,将会给肿瘤学研究带来更精准的结果,也会促进干细胞等药物的再生医学研究。
获取更多SRG大鼠模型技术支持,可咨询维通利华产品经理:
产品咨询:Product@criver.cn
订购电话:010-84744555
订购邮箱:Order@criver.cn